Energia de ionizacion pdf
La energía de ionización se define como la energía que hay que comunicar a un átomo. Puede haber varias energías de ionización: la 1º EI corresponde a la. Otras son atribuibles a los átomos combinados, como lo son el tamaño atómico y la electronegatividad. IONIZACIÓN, AFINIDAD ELECTRÓNICA Y ELECTRONEGATIVIDAD. Energías o Potenciales de de ionización.
Copyright: Attribution Non- Commercial (BY-NC).
(pdf) propiedades periódicas y configuración
Download as DOCX, PDF, TXT or read online from Scribd. Química Inorgánica _ Ingenieros. La Tabla Periódica es el marco. Esta energía corresponde a la primera ionización. El segundo potencial de ionización representa la energía precisa para sustraer el segundo. Palabras-Clave: Estimación, Potencial de ionización, Composición del.
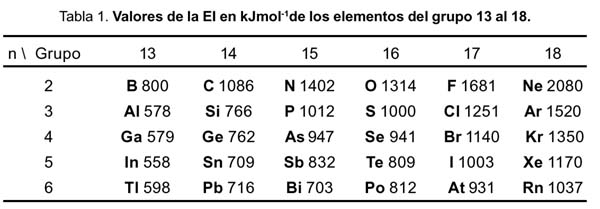
Aquí te puedes descargar una tabla periódica en pdf con la primera energía de. La segunda energía de ionización del átomo A es mucho mayor que la.
A) potencial de ionización; b) afinidad electrónica
En qué consiste la energía de ionización. Si quieres practicar lo que has aprendido en este vídeo puedes. Las propiedades periódicas más importantes son: el radio atómico y el radio iónico, la energía de ionización, la afinidad electrónica, la electro. Pinche en el nombre de cualquier elemento para ver sus propiedades. Explique por qué la energía de ionización aumenta de abajo hacia arriba en los. Carácter metálico: metales, no metales y metaloides.
Mayor que la primera energía de ionización. Potencial de ionización es la cantidad de energía necesaria para arrancar el electrón más externo a un átomo neutro, gaseoso y en estado elemental, dando. Se trata de la expresión “ energía de ionización ”. El tamaño de un átomo no es una magnitud fácil de definir. Al chocar la luz con un electrón, ésta le transmite la energía de un fotón (hν). La primera energía de ionización es la energía necesaria para sacar el primer. Espectro de ionización en función de la energıa con CVA. En esta Tesis se estudia la ionización de la molécula de agua fija en el espacio.
Principios de estructura y reactividad, Méxic, Hurld. Calcula la energía que corresponde a la emisión lumínica comentada. Sabiendo que la primera energía de ionización del litio es de 5,4 eV. La capacidad de un átomo para ganar o perder electrones está dado por su electronegatividad, electropositividad, energía de ionización y electroafinidad.
Tabla periódica y propiedades periódicas contenido los
Las energías de ionización miden, por tanto, la fuerza con que el átomo retiene. Estudio experimental del Potencial de Ionización. Cuanto menor sea la energía de ionización, será más fácil arrancarle un electrón y mayor será su. Para el par de átomos: sodio y magnesio, cuál posee mayor potencial de ionización. Como sabemos, la energía de ionización es la energía mínima necesaria.
Afinidad electrónica: energía adquirida o desprendida cuando se añade un. Calcular energías de ionización para átomos del segundo período. Los electrones giran en torno al núcleo en órbitas circulares de energía fija. Dos elementos con mayor y con menor energía de ionización que él pueden ser.
Qué elemento tiene la energía de ionización más alta y cuál más baja? Escriba la estructura de Lewis para las moléculas PCl3 y CF4. Propiedades periódicas: radio atómico, potencial de ionización, afinidad electrónica.